近日,海南普利制藥股份有限公司收到美國食品藥品監督管理局(以下簡稱“FDA”)簽發的拉考沙胺注射液的上市許可,標志著普利制藥具備在美國銷售拉考沙胺注射液的資格,將對公司拓展美國市場帶來積極影響,這是2024年普利制藥獲得的第5張海外批件,也是繼伏立康唑干混懸劑、阿昔洛韋鈉注射液后獲得的美國第3張ANDA批件。同時,拉考沙胺注射液也在我國審評審批中。

一、藥品基本情況
藥品名稱:拉考沙胺注射液
適應癥:(1)4歲及以上患者部分發作性癲癇的治療;(2)4歲及以上患者原發性全身性強直-陣攣性癲癇的輔助治療。
劑型:注射劑
規格:200mg/20mL
ANDA號:217311
生產企業:海南普利制藥股份有限公司

第三代抗癲癇藥物,市場前景廣闊
癲癇是常見的慢性中樞神經系統疾病之一,全球癲癇患者人數超過6500萬。目前抗癲癇藥物(AEDs)是控制癲癇發作的主要手段,自20世紀90年代初以來,許多新型AEDs已進入市場,其在藥動學、療效、安全性及藥物相互作用等方面優勢顯著。
拉考沙胺為第三代新型AEDs,最早由UCB制藥研發,2008年8月UCB開發的原研藥拉考沙胺注射液Vimpat首先在歐盟批準上市,2008年10月獲準在美國上市。拉考沙胺是一系列功能性氨基酸中的一種,在不同的臨床前模型和臨床研究中顯示出具有抗癲癇作用。在體外電生理研究表明,拉考沙胺選擇性增加電壓門控鈉通道的慢失活,導致對過度興奮的神經元細胞膜的穩定作用。
根據IMS數據顯示,2023年拉考沙胺注射劑型全球銷量近320萬支,其中美國市場占據23%,為全球第二大市場,用藥經驗豐富,臨床療效受認可,市場前景廣闊。
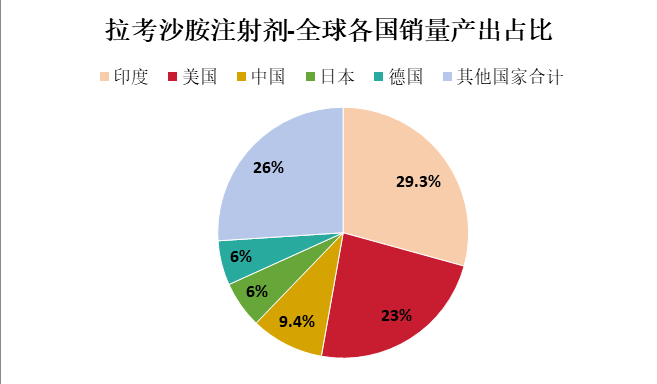
圖1:【拉考沙胺注射劑】全球各國銷量產出占比
合作聯系
歡迎大家一起開拓全球市場
Welcome to explore the global market together
聯系人:周先生

 首頁
首頁









